表示しようとしているページは、医療関係者向け「コンドリアーゼ適正使用情報」のページです。
医療関係者向けページのご利用は、日本国内の医療関係者の方に限らせていただきます。
日本国外の医療関係者、一般の方への情報提供を目的としたものではありません。
あなたは医療関係者ですか?
コンドリアーゼ適正使用情報のページでご覧いただける情報は以下です。
- 適正使用に関する情報
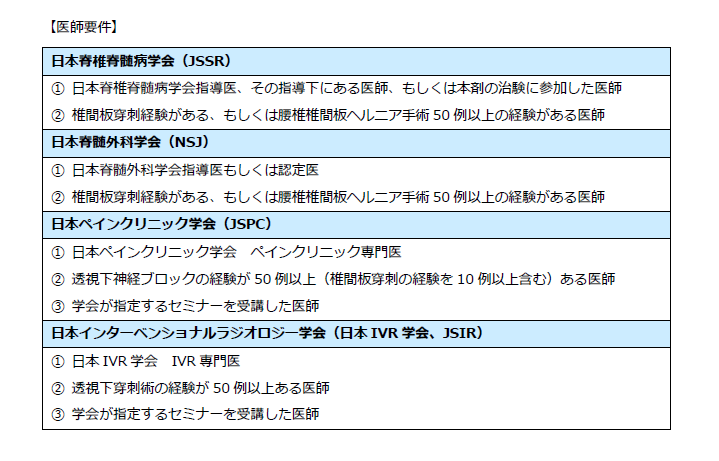
- 本剤の使用要件
- 関連学会
ヘルニコア®椎間板注用1.25単位は、2018年3月に本邦で初めて承認された椎間板内酵素注入療法に用いる椎間板内投与の薬剤です。安全確保のため添付文書における「使用上の注意」として、「本剤の投与は、腰椎椎間板ヘルニアの診断及び治療に十分な知識・経験を持つ医師のもとで行うこと。また、椎間板穿刺に熟達した医師が投与すること。」及び「本剤の投与に際しては、ショック、アナフィラキシー等の発現のおそれがあるので、救急処置のとれる準備をしておくこと。投与終了後も十分な観察を行い、症状が発現した場合には直ちに適切な処置を行うこと。」が求められています。
これら「使用上の注意」に関する適正な使用を推進するため、本剤の適正使用ガイドに記載のとおり、日本脊椎脊髄病学会、日本脊髄外科学会、日本ペインクリニック学会又は日本インターベンショナルラジオロジー学会において要件が設定されております。
本剤の納入に際しては、科研製薬株式会社より上記学会の要件を満たすことを確認させていただきますので、ご協力の程よろしくお願いいたします。
添付文書
医薬品リスク管理計画(RMP)
医療従事者向資材 適正使用ガイド
患者向資材 冊子『ヘルニコアの治療を受けられる方へ』
-
 一般使用成績調査及び特定使用成績調査 安全性に関する中間集計結果
(288KB)
一般使用成績調査及び特定使用成績調査 安全性に関する中間集計結果
(288KB)