生化学工業は、有用で高品質な医薬品・医療機器を継続的に患者の方々に提供することを使命とし、法令や基準に対応できる品質保証・信頼性保証体制を構築しています。
当社は、GxP※と呼ばれる各種基準を含む各国の薬事法規制を遵守することにより、研究開発から製造販売後まですべての段階において、品質及び信頼性の確保に最大限注力しています。国内では、「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(薬機法)」に基づき、製造販売業者として三役体制(総括製造販売責任者、品質保証責任者、安全管理責任者)を構築し、適切な品質管理及び安全管理業務を行っています。
今後も世界中の患者の方々が求める医薬品・医療機器を確実に提供し続けるために、最新の規制動向に対応できる、グローバル基準の品質保証・信頼性保証体制の維持・向上に努めていきます。
※GxP:Good *** Practice(適正***基準)の略。医薬品・医療機器の研究開発段階から発売後の有効性、安全性、品質の信頼性等を確保するために定められた各基準の総称。
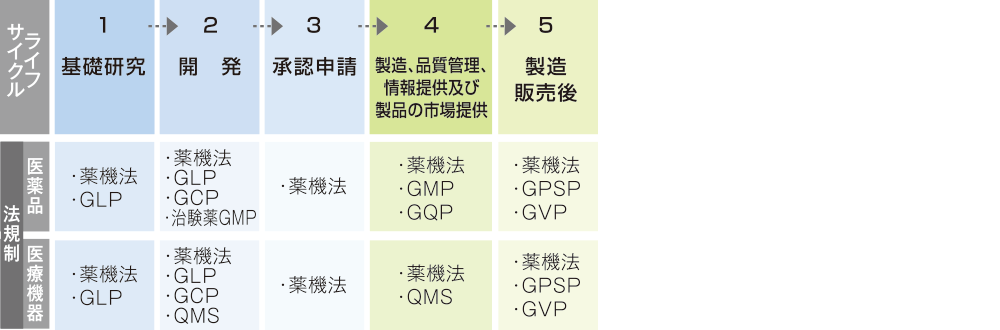
- 薬機法:医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律
- GLP:Good Laboratory Practice、安全性に関する非臨床試験の実施の基準
- GCP:Good Clinical Practice、臨床試験の実施に関する基準
- GMP:Good Manufacturing Practice、製造における製造管理、品質管理の基準
- GVP:Good Vigilance Practice、製造販売後の安全管理基準
- GQP:Good Quality Practice、製品の品質管理の基準
- GPSP:Good Post-marketing Study Practice、製造販売後調査・試験の実施の基準
- QMS:Quality Management System、医療機器及び体外診断用医薬品の製造管理及び品質管理の基準に関する省令
当社は、高品質な医薬品・医療機器を安定的に供給するために、「品質方針」に基づき、世界に通用する品質マネジメントシステムを構築しています。開発段階では安全性に関する非臨床試験の実施基準及び臨床試験の実施基準に基づき信頼性を保証しています。また、販売後には、法規制の遵守や品質保証体制の維持を担保するために、毎年計画的に自己点検や内部監査を実施し、品質マネジメントシステムの運用状況を確認するとともに、必要に応じて是正措置・予防措置を迅速に講じています。
さらに当社は、ヒアルロン酸ナトリウムを素材とした変形性膝関節症及び肩関節周囲炎治療用粘弾性製品の開発、製造および販売に関して、ISO13485の認証を取得しています。当社はこれらの製造管理及び品質保証システムに則って、製品の設計開発から販売後の段階まで、品質を厳密に維持・管理しています。
ISO13485は、国際標準化機構(International Organization for Standardization)によって定められた、医療機器の設計・開発、製造などの要求事項を規定した国際的な品質マネジメントシステムの規格です。日本においては、医療機器及び体外診断用医薬品の製造管理及び品質管理の基準に関する省令にも採用されています。
医薬品の販売後には、開発段階では予測できなかった副作用等が明らかになることがあります。当社は製造販売後の安全管理基準(GVP)を遵守し、医療現場で処方された医薬品に関する副作用情報等を迅速かつ適正に収集・評価し、フィードバックするファーマコビジランス(医薬品安全性監視)活動を実施しています。これらの活動により、副作用の拡大を未然に防止し、医薬品に関する安全性確保と適正使用を推進しています。
当社ではメディカル活動推進室を設置し、販売部門から独立して、社外専門家に最新の科学的知見を提供する活動を推進しています。高い倫理性と科学的専門性のもと、当社が取り扱う運動器領域や眼科領域などの疾患情報及び製品に関する医学的エビデンスを創出、発信することで、医療の発展に貢献しています。