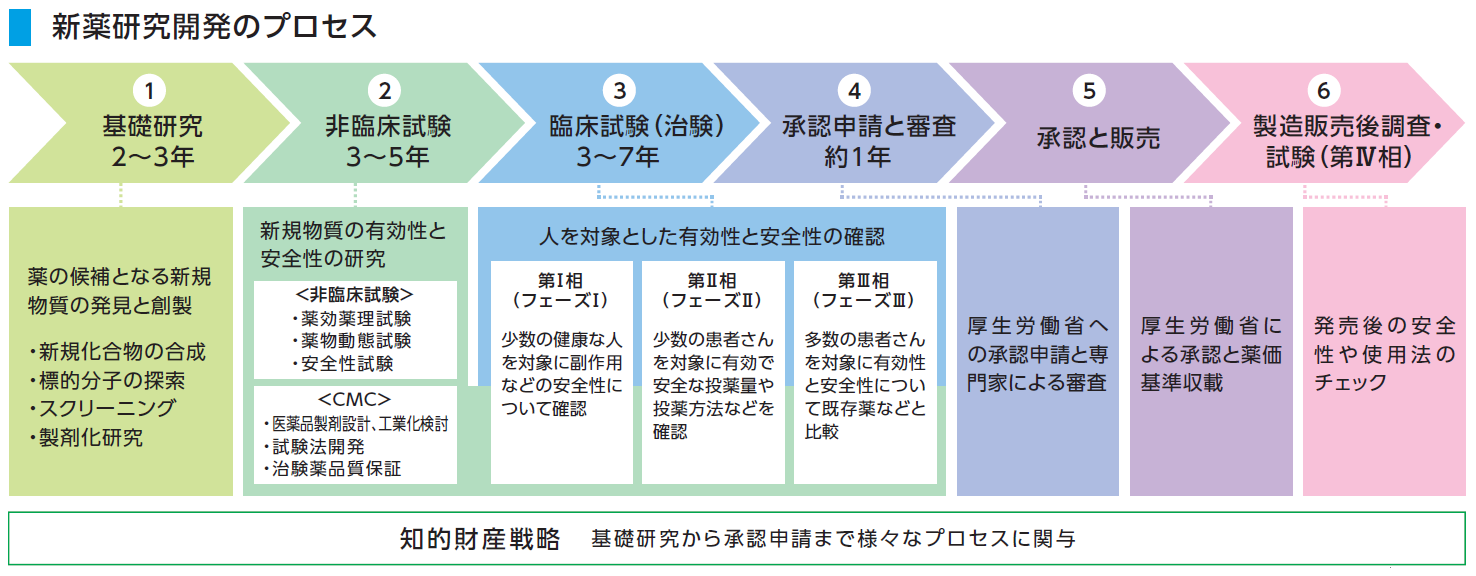
新しい薬を創るためには様々な試験を行い、有効性や安全性を評価する必要があります。臨床試験(治験)とは、基礎研究、非臨床試験などの研究過程を経て、薬の候補が実際に人に役立つかどうかを確認する試験のことです。 臨床試験は、通常3つのステップに分けられ、厳しい基準に従って、病院などの医療機関において被験者(健康な人や患者の方々)の同意を得たうえで行われます。
最初のステップである第Ⅰ相臨床試験(フェーズⅠ)は、通常、少数の健康な方々を対象に被験薬の薬物動態(吸収、分布、代謝、排泄)や安全性(有害事象、副作用)について検討することを主な目的として実施されます。次の第Ⅱ相臨床試験(フェーズⅡ)では、少数の患者の方々を対象として有効性・安全性・薬物動態などを検討し、有効で安全な投薬量や投薬方法を確認します。最後の第Ⅲ相臨床試験(フェーズⅢ)では、多くの患者の方々を対象に既存薬などとの比較試験等を実施して、有効性と安全性についての客観的な検証を行います。
薬の候補物質の発見から、新薬として承認を取得するまでには、一般的に10年以上の期間を要します。臨床試験は、この長く厳しい新薬開発の過程の中で承認を申請できるかの鍵を握る重要なステップといえます。